URL: https://www.desy.de/infos__services/presse/pressemeldungen/2012/pm_011212/index_ger.html
Breadcrumb Navigation
Röntgenanalyse enthüllt Hauptschalter mit wichtiger Rolle bei Hautkrebs
Vielversprechender Ansatz für die Entwicklung neuartiger Medikamente
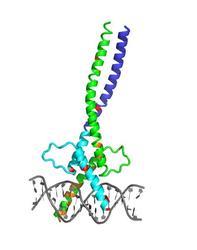
Struktur des Mikrophthalmie-assoziierten Transkriptionsfaktors MITF. Deutlich erkennbar ist der neu entdeckte Knick. Strukturelle Veränderungen durch Mutationen bei Menschen (Tietz- oder Waardenburg-Syndrom) sind rot markiert, solche bei der Maus in Orange. Bild: Vivian Pogenberg, EMBL Hamburg
Hamburg, 1. Dezember 2012. Mit dem Röntgenblick von DESYs Forschungslichtquelle DORIS haben Forscher aus Hamburg und Island die Struktur eines zentralen molekularen Schalters entschlüsselt, der eine wichtige Rolle bei der gefährlichsten Form von Hautkrebs spielt, dem Melanom. Die Ergebnisse, die in der Dezemberausgabe des Fachjournals "Genes & Development" erscheinen, werfen ein neues Licht auf die Funktion des sogenannten Mikrophthalmie-assoziierten Transkriptionsfaktors MITF.
MITF wird nicht nur mit Hautkrebs in Verbindung gebracht, sondern auch mit verschiedenen Erbkrankheiten, bei denen die Produktion des Hautpigments Melanin gestört ist. Es spielt auch eine Rolle bei manchen Aspekten des Alterns. "Unsere Ergebnisse können eine rationale Grundlage für die Entwicklung maßgeschneiderter Wirkstoffe liefern, die an MITF angreifen", erläutert Erstautor Vivian Pogenberg von der Hamburger Auβenstelle des Europäischen Molekularbiologie-Labors EMBL.
Das Melanom (schwarzer Hautkrebs) ist ein bösartiger Tumor der pigmentproduzierenden Zellen. Diese sogenannten Melanozyten stellen das Hautpigment Melanin her. Das Melanom ist zwar nicht die häufigste Form von Hautkrebs, aber die mit der höchsten Todesrate: Rund drei von vier Hautkrebs-Todesfällen gehen auf Melanome zurück. Eine wichtige Rolle bei der Entwicklung von Melanomen spielen Fehlfunktionen im Mikrophthalmie-assoziierten Transkriptionsfaktor MITF. Allgemein steuern Transkriptionsfaktoren welche Teile des Erbguts in einer Zelle abgelesen und in Baupläne für Proteine umgesetzt werden. In einer einzelnen Zelle ist jeweils zu einer bestimmten Zeit nur ein kleiner Teil aller Gene aktiv.
MITF aktiviert beispielsweise die zelleigene Maschinerie, um aus der Aminosäure Tyrosin das Pigment Melanin zu produzieren. Aber der Transkriptionsfaktor sorgt auch dafür, dass aus Stammzellen überhaupt erst Melanozyten werden. Er spielt eine wichtige Rolle bei der Vermehrung und beim Tod von Pigmentzellen. Aus diesem Grund wird MITF auch als Hauptschalter bezeichnet. Zusätzlich hat er Aufgaben in anderen Zelltypen wie den Mastzellen des Immunsystems oder den "Knochenfressern", den Osteoklasten.
MITF-Mutationen spielen nicht nur eine Rolle bei der Entstehung von Hautkrebs, sondern führen auch zu schweren Erbkrankheiten wie dem Tietz- oder dem Waardenburg-Syndrom, die mit Taubheit, Haut- und Haarpigmentierungsstörungen, Augenfehlbildungen und Sehstörungen einhergehen. Der Transkriptionsfaktor ist auch an altersbedingten Pigmentierungsstörungen wie dem Ergrauen der Haare beteiligt.
Die Forscher um Pogenberg und EMBL-Gruppenleiter Matthias Wilmanns ließen im Labor kleine Proteinkristalle aus MITF wachsen und durchleuchteten diese mit dem Röntgenlicht von DORIS. Dabei entsteht kein klassisches Röntgenbild, sondern die Kristalle streuen die Röntgenstrahlung auf charakteristische Weise. Aus dem Streubild lässt sich mathematisch die Struktur des Kristalls rekonstruieren und damit die Struktur von MITF. Die Analyse enthüllte ungewöhnliche Veränderungen in dem Molekül, die ihm einen charakteristischen Knick verleihen. MITF bildet ein Doppelmolekül (Dimer) mit langen Spiralen, die wie ein Reißverschluss ineinandergreifen. Der charakteristische Knick in diesem Reißverschluss führt dazu, dass MITF sich kaum an andere Transkriptionsfaktoren binden kann.
Die Forscher konnten auch Strukturänderungen in dem Molekül identifizieren, die auf eine Reihe von bekannten MITF-Mutationen zurückgehen, die etwa zu bestimmten Fellfarben bei Mäusen und zu Tietz- oder Waardenburg-Syndrom beim Menschen führen. Die verschiedenen MITF-Formen steuerte das Labor von Ko-Autor Eiríkur Steingrímsson an der Universität von Island bei, das eine große Bibliothek verschiedener MITF-Mutationen besitzt. Steingrímsson war auch maßgeblich an der Interpretation der Daten beteiligt.
Mit den MITF-Strukturinformationen von DORIS konnten die Wissenschaftler an der Europäischen Synchrotronstrahlungsquelle ESRF im französischen Grenoble die Verbindung zwischen MITF und der DNA untersuchen. Die Analyse zeigte unter anderem Strukturänderungen durch die namensgebende Mutation, die zu weißem Fell und unnatürlich kleinen Augen (Mikrophthalmie) bei Mäusen führt. Es zeigte sich, dass diese Strukturänderungen die Bindungsstelle zwischen MITF und der DNAbeeinflussen, wodurch der Transkriptionsfaktor schlechter an die DNA andockt. Andere Mutationen führen wiederum dazu, dass MITF an zu viele Gene binden kann und so an falschen Stellen andockt.
"Das Fernziel ist, die MITF-Funktionsweise komplett zu verstehen, um zu beurteilen, wie es sich für mögliche Therapien eignet", betont Wilmanns. "Ein möglicher Weg könnte beispielsweise sein, mit maßgeschneiderten Molekülen gezielt die Dimerisierung von MITF in Melanozyten zu stoppen", erläutert Pogenberg. "Alternativ könnte ein anderes passgenaues Molekül den Transkriptionsfaktor daran hindern, die Bindestelle im Erbgut zu erkennen."
Originalveröffentlichung
"Restricted leucine zipper dimerization and specificity of DNA recognition of the melanocyte master regulator MITF"; Vivian Pogenberg et al.; "Genes & Development", 2012; DOI: 10.1101/gad.198192.112
Wissenschaftlicher Ansprechpartner
Dr. Matthias Wilmanns, EMBL Hamburg, +49 40 89902-126, matthias.wilmanns@embl-hamburg.de
Prof. Eirikur Steingrimsson, University of Iceland, +354 525 4270, eirikurs@hi.is
Pressekontakt
DESY-Sprecher Thomas Zoufal, +49 8998-1666, presse@desy.de
EMBL-Hamburg-Sprecherin Dr. Rosemary Wilson, EMBL Hamburg, +49 40 89902-228, r.wilson@embl-hamburg.de
Mikroskopaufnahme der untersuchten MITF-Kristalle. Bild: Vivian Pogenberg/EMBL Hamburg